
2025年10月20日,诗健生物在2025年ESMO会议上以Poster形式公布了ESG401(Trop2 ADC)一线治疗转移性三阴性乳腺癌的最新临床数据。早在2024年11月,ESG401在该适应症已获得国家药品监督管理局药品审评中心(CDE)的突破性治疗药物认定。
研究题目:Updated Efficacy of Anti-TROP2 ADC ESG401 for First-Line Metastatic TNBC.
研究背景:
ESG401是一种新型的ADC,由人源化Trop-2单抗通过稳定可裂解连接子与SN38偶联而成,药物抗体偶联比(Drug Antibody Ritio, DAR)为8。该药物在经多线治疗的转移性乳腺癌(mBC)中已显示出疗效,但其在一线治疗转移性三阴性乳腺癌(mTNBC)中的应用数据,尤其是单药治疗的数据,仍较为有限。本报告更新了一项1a/1b期研究(NCT04892342)中一线治疗mTNBC队列的最新结果。
研究方法:
本研究入组患者为年龄≥18岁、经组织学确诊的局部晚期/不可切除或转移性三阴性乳腺癌,且既往未针对局部复发无法手术或转移性乳腺癌进行过系统性抗肿瘤治疗。患者接受ESG401(16 mg/kg,静脉注射,第1、8、15天给药,28天为一周期)治疗,直至疾病进展、出现不可耐受的毒性或撤回知情同意。
研究结果:
入组情况及基线特征
截至2025年6月30日,40名患者接受了至少1次ESG401治疗。入组患者的年龄中位值为54岁(范围:33,73)。20%的患者为初诊IV期。基线时58%的患者伴有肺转移,38%的患者伴有肝转移,8%的患者伴有脑转移;25%的患者接受过新辅助化疗,78%的患者接受过手术,68%的患者接 受过辅助化疗,38%的患者接受过放疗。
安全性
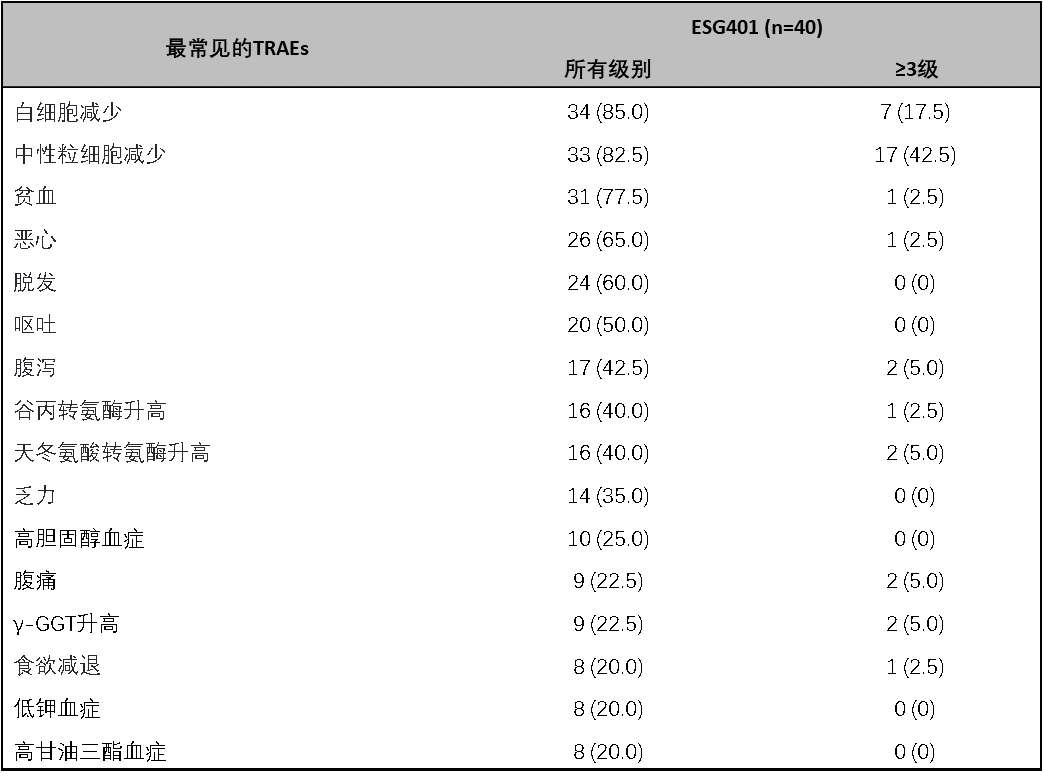
安全性特征与既往报告一致,未出现新的或非预期的安全信号。最常见的≥3级与研究药物相关的不良事件(TRAEs)包括中性粒细胞计数降低、白细胞计数降低。
有效性
接受ESG401一线治疗mTNBC的40例患者中,疗效可评估的受试者共35例,其中有3例受试者疗效评价达到CR。ORR为82.9%,DCR为100%,中位PFS值为13.0个月,中位DOR为18.8个月。
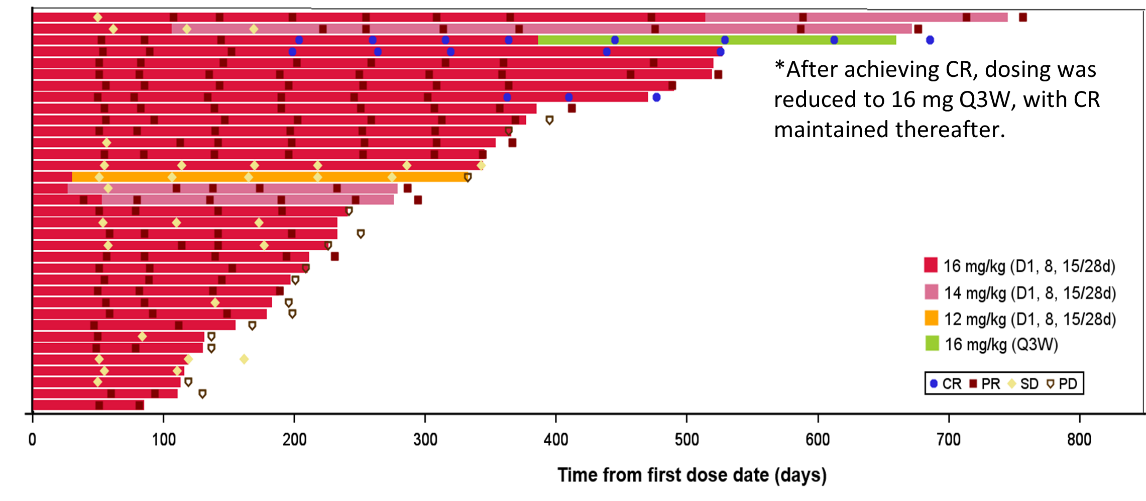
图1. 所有疗效可评估受试者游泳图
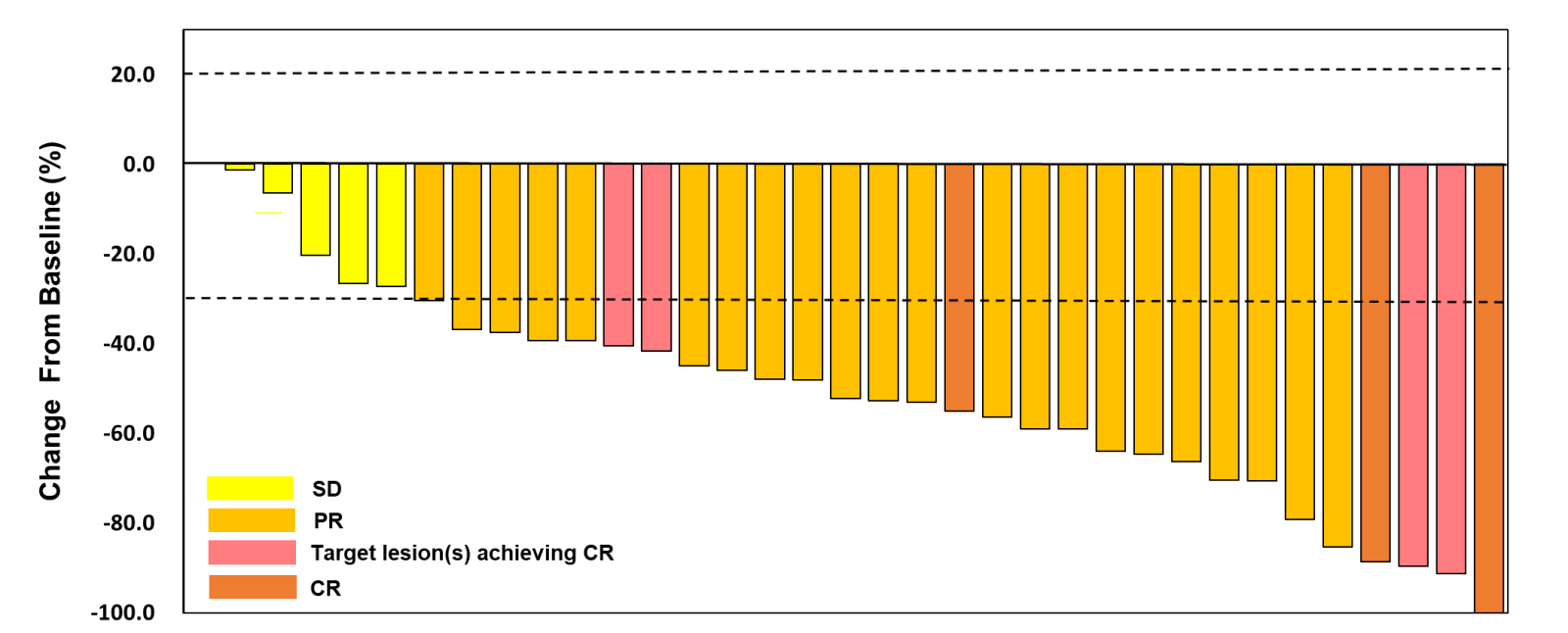
图2. 靶病灶直径总和(SOD)最佳百分比变化瀑布图

图3.无进展生存期(PFS)K-M曲线图
亮点总结:
本次ESMO会议上,吉利德和阿斯利康/第一三共也分别公布了Sacituzumab Govitecan (ASCENT-03研究)、Dato-DXd(TROPION-Breast02研究)一线治疗三阴乳腺癌(TNBC)的三期临床研究结果。笔者整理如下:

ESG401在ESMO会议壁报展示的poster原文如下:
